El sector sanitario está experimentando una rápida transformación impulsada por la llegada de tecnología de diagnóstico médico avanzada. El desarrollo de software IVD es un componente fundamental de esta revolución, ya que permite realizar pruebas, análisis, informes y comunicación sin necesidad de un laboratorio físico ni de una visita al consultorio médico.
Llevar el desarrollo de software IVD al mercado puede beneficiar a los pacientes y a los proveedores de atención médica, que pueden brindar atención de calidad más rápido y con menos recursos.
Tamaño proyectado del mercado de IVD en todo el mundo de 2018 a 2027 (en millones de dólares estadounidenses)
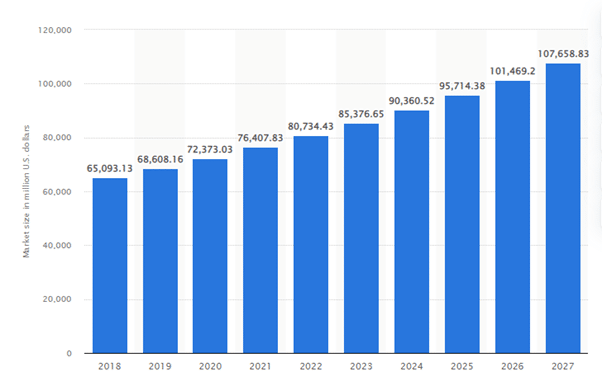
Fuente: statista
El gráfico anterior muestra que el mercado de diagnóstico in vitro (IVD) a nivel mundial se estimó en 72 400 millones de dólares estadounidenses en 2020, con un crecimiento proyectado de 108 000 millones de dólares estadounidenses para 2027, lo que demuestra su mayor relevancia en el sector sanitario actual.
1. Realizar estudios de mercado
Antes de iniciar el proceso de desarrollo, las organizaciones deben realizar estudios de mercado y comprender su mercado objetivo, las necesidades de los usuarios y los posibles competidores.
La investigación de mercado también debería ayudar a determinar los requisitos reglamentarios que las organizaciones deben cumplir y las tendencias actuales dentro del sector o el espacio tecnológico.
A continuación, se indican algunos puntos clave que debe tener en cuenta al realizar estudios de mercado para el desarrollo de software IVD:
- Identificar los requisitos reglamentarios: Identificar los requisitos reglamentarios de su software es esencial para comercializar su producto. Pueden variar en función de su mercado objetivo, como la FDA en los EE. UU. o los requisitos de marcado CE de la Unión Europea (IVDR 746/2017).
- Determinar su mercado objetivo: Identifique los segmentos del sector sanitario a los que servirá su software IVD. Tenga en cuenta factores como la geografía, el tipo de organización sanitaria y las áreas de especialidad.
- Identificar a sus competidores: Investigue el mercado de software IVD para identificar a sus competidores y sus productos. Analice sus puntos fuertes, débiles, precios y estrategias de marketing.
- Comprender a sus clientes: Realice encuestas, entrevistas y grupos focales con profesionales sanitarios para comprender sus necesidades, preferencias y puntos débiles. Utilice esta información para adaptar su software IVD a sus necesidades específicas.
- Analizar las tendencias del mercado: Manténgase al día de las últimas tendencias y novedades en el mercado de software IVD. Supervise las publicaciones del sector, asista a conferencias y siga a expertos del sector y líderes de opinión en las redes sociales.
- Determinar la estrategia de precios: Tenga en cuenta los costes, el mercado objetivo y la competencia al determinar la estrategia de precios, por ejemplo, una tarifa única. ¿Cuota de suscripción? ¿Tarifa por prueba?
2. Clasificación del software IVD
Comprender la clasificación de su software IVD es fundamental antes de iniciar el proceso de planificación y diseño. Determine si el software IVD es un dispositivo médico IVD independiente o un componente de un sistema más grande. Para ser calificado como software de dispositivo médico IVD en la UE, el producto debe cumplir con la definición de IVD de acuerdo con el Artículo 2(2) del Reglamento IVDR 746/2017, como se describe en la Figura 1. La clasificación correcta del software IVD debe realizarse en función de las reglas descritas en el Anexo VIII del IVDR. Los documentos de orientación pertinentes, como MDCG 2019-11, también son esenciales para la calificación y clasificación del software IVD.
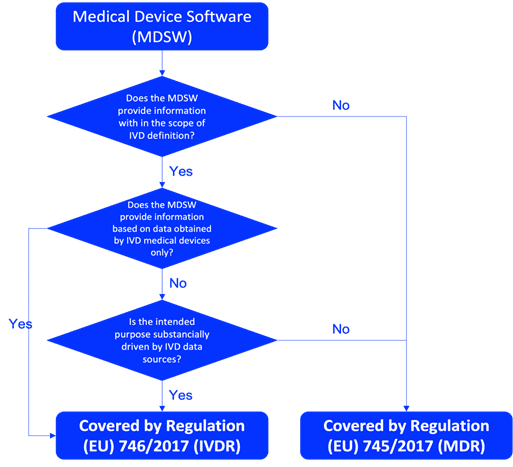
Fig. 1: Diagrama de flujo de MDCG 2019-11 sobre la calificación del software de dispositivos médicos (MDSW)
Familiarícese con los marcos regulatorios, las guías y los estándares relevantes, como ISO 13485, IEC 62304, pero también con los documentos de guía específicos publicados por los reguladores, que brindan especificaciones y pautas para desarrollar, validar y mantener el software IVD.
3. Planificar y diseñar el software
El siguiente paso crucial para un desarrollo de software IVD exitoso es el diseño y la planificación.
- Un proceso de planificación sólido y bien documentado puede ayudar a proporcionar una hoja de ruta más detallada para el desarrollo.
- Durante esta fase, las revisiones de diseño, las pruebas y la verificación garantizarán que la versión final cumpla con los requisitos del usuario.
- Es esencial incorporar los comentarios de los usuarios en cada etapa del proceso de diseño para desarrollar una interfaz intuitiva que funcione eficazmente de acuerdo con sus necesidades.
- Obtener comentarios de los clientes y las partes interesadas ofrece al equipo de desarrollo oportunidades para reconocer posibles inquietudes y áreas de mejora.
- Los desarrolladores pueden idear soluciones de software que satisfagan las necesidades de los clientes y aborden sus quejas integrando los comentarios.
- No se debe subestimar la importancia de una documentación precisa, ya que ayuda a rastrear los problemas más adelante en el ciclo de vida del software.
- El equipo de desarrollo debe tener en cuenta la escalabilidad y la flexibilidad durante las etapas iniciales de planificación y diseño al crear el software.
4. Desarrollar y probar el software
Desarrollar y probar el software es crucial para crear un prototipo funcional.
- La fase de desarrollo es necesaria para garantizar la precisión del diseño, la codificación y los algoritmos utilizados en la creación de las soluciones de software.
- Las pruebas y el control de calidad también desempeñan un papel esencial para garantizar que los productos cumplan con todos los requisitos antes del lanzamiento.
- Es esencial que las empresas evalúen minuciosamente cada componente de su software como parte de este proceso. Esto incluye garantizar que cumplan con los objetivos de rendimiento con respecto a la velocidad, la capacidad de respuesta, la escalabilidad, la seguridad, la fiabilidad y la facilidad de uso para sus usuarios.
- Los controles de garantía de calidad ayudan a identificar errores o fallos para lanzar un producto sin defectos que cumpla con todos los estándares de organismos reguladores como la FDA o el marcado CE.
- Al implementar sistemas IVD, los fabricantes deben considerar si sus aplicaciones pueden ser lo suficientemente flexibles para admitir nuevos avances tecnológicos; la preparación para el futuro de sus productos se vuelve cada vez más necesaria donde los clientes exigen longevidad en las actualizaciones o iteraciones a lo largo del tiempo.
5. Preparar una presentación reglamentaria
Preparar un paquete de presentación reglamentaria es fundamental para comercializar el desarrollo de software IVD. Este paso implica la recopilación de documentos para demostrar que el software cumple con los requisitos reglamentarios y es seguro y eficaz.
Estas son algunas consideraciones críticas para preparar una presentación reglamentaria:
- Recopilar los documentos pertinentes para el paquete
Comprender las regulaciones, los estándares y la clasificación de riesgo del software IVD y el rol de fabricación. Los documentos clave que se deben incluir son la descripción del dispositivo, la documentación técnica, el archivo de gestión de riesgos (ISO 14971), la documentación del ciclo de vida del software (IEC 62304) y la documentación del sistema de gestión de calidad (ISO 13485). La gestión de riesgos debe aplicarse y supervisarse durante el ciclo de vida del desarrollo de software IVD.
- Preparar un informe de evaluación del rendimiento (PER)
Esto requerirá un análisis exhaustivo de la evidencia científica que demuestre que el producto satisface las necesidades del usuario de forma segura y eficaz. La evaluación del rendimiento del software IVD debe prepararse de acuerdo con los documentos de orientación pertinentes, como
Los estudios de rendimiento clínico tienen como objetivo proporcionar evidencia de la seguridad y eficacia del propósito previsto de un producto para garantizar que pueda diagnosticar, controlar y predecir enfermedades y afecciones con precisión.
Como se describe en MDCG 2020-1 “La validación del rendimiento clínico debe considerarse en cada cambio del software a una nueva versión. Si no se realiza ninguna validación, se debe indicar una justificación en la documentación técnica. Con una validación del rendimiento clínico, se demuestra que los usuarios pueden lograr resultados clínicamente relevantes a través del uso predecible y fiable del MDSW”.
La adhesión a las normas y directrices pertinentes, como ISO 20916 (Estudios de rendimiento clínico para diagnósticos in vitro) y las buenas prácticas clínicas (CGP), es crucial para la ejecución exitosa de los estudios clínicos.
- Garantizar la precisión de los datos
Asegúrese de que todos los datos recopilados de las pruebas se presenten con precisión para demostrar la seguridad y la eficacia antes de enviar su solicitud. Esto incluye los datos de validación y verificación, las evaluaciones de rendimiento y, si corresponde, los resultados de los estudios clínicos. Revise cuidadosamente toda la información para verificar su exactitud e integridad antes de enviarla.
6. Obtener la aprobación reglamentaria
Debe obtener la aprobación reglamentaria para comercializar el desarrollo de software IVD. Una aprobación exitosa le permite comercializar y vender su software de conformidad con las leyes y regulaciones locales.
- Familiarícese con los marcos y directrices regulatorias aplicables para su software. Estos pueden incluir ISO 13485 (sistemas de gestión de calidad), IEC 62304 (procesos del ciclo de vida del software de dispositivos médicos), ISO 14971 (gestión de riesgos) y documentos de orientación de MDCG como MDCG 2019-11 (calificación y clasificación del software en las regulaciones de dispositivos médicos) y MDCG 2020-1 (guía sobre la evaluación del rendimiento para el software IVD según el IVDR. También debe considerar las directrices de otras jurisdicciones según su estrategia de mercado. La FDA, por ejemplo, ha emitido guías para el software como dispositivo médico (SAMD).
- Desarrolle un paquete de solicitud integral que incluya todos los documentos, datos y pruebas necesarios para la revisión. Asegúrese de que su paquete aborde los requisitos reglamentarios, como los procedimientos de evaluación de la conformidad, la evidencia clínica y la vigilancia posterior a la comercialización.
- Envíe el paquete de solicitud a las autoridades reguladoras pertinentes para su revisión, como la FDA en los EE. UU. o los organismos notificados en la UE en virtud del Reglamento de diagnóstico in vitro (IVDR) 2017/746.
- Esté preparado para responder de forma rápida y precisa a cualquier comentario o solicitud de información adicional de las agencias reguladoras durante el proceso de revisión.
- Realice los cambios recomendados rápidamente como parte de su presentación para obtener la aprobación de las agencias con éxito.
- Una vez que reciba la aprobación de las agencias reguladoras, puede seguir adelante con la comercialización y venta de su software de acuerdo con las leyes y regulaciones locales, asegurando el cumplimiento continuo de cualquier requisito posterior a la comercialización.
7. Desarrollo de estrategias de marketing y ventas
Crear una estrategia de marketing y ventas exitosa es esencial para llevar el software IVD al mercado, ya que permite un posicionamiento más rápido y obtener una ventaja competitiva. Asegúrese de desarrollar una identidad de marca sólida con mensajes que resuenen con su audiencia.
Además, investigar las necesidades de los clientes y comprender las tendencias clave de la industria puede crear un enfoque más específico cuando se trata de la comercialización de soluciones de software IVD, lo que aumenta su probabilidad de éxito.
Asegúrese de utilizar múltiples canales, como publicidad de pago, campañas de correo electrónico, redes sociales y seminarios web, para llegar a clientes potenciales de diversos segmentos.
Y, por último, pero no menos importante, la creación de estrategias de comunicación eficaces para interactuar con los clientes durante todo el ciclo de ventas también será clave para promocionar los productos IVD con éxito.
8. Lanzar y dar soporte al software
Lanzar y dar soporte al software es un elemento crucial para su éxito. El producto se puede mejorar con el tiempo proporcionando actualizaciones periódicas y servicio al cliente, y los usuarios pueden obtener la mejor experiencia.
Estos son algunos puntos que debe tener en cuenta al lanzar su desarrollo de software IVD:
- Cree un plan de soporte integral que ponga las necesidades del cliente en primer lugar. Asegúrese de tener un proceso eficiente para gestionar las consultas y los problemas técnicos a medida que surjan.
- Asegúrese de que todas las actualizaciones de software necesarias se completen según lo programado, para que los usuarios no experimenten ningún retraso en el acceso a las funciones completas del producto o las correcciones de errores.
- Evalúe el impacto regulatorio de los cambios y las correcciones de errores, los cambios en su software IVD pueden ser o no significativos. Considere si los cambios impactan sus aprobaciones regulatorias. MDCG 2022-6 proporciona orientación adicional sobre los cambios en el diseño y el propósito previsto en el contexto de los nuevos plazos de transición para los IVD en Europa.
- Configure formularios de comentarios de los usuarios o encuestas para que los clientes puedan compartir sus opiniones sobre el rendimiento del producto y las mejoras que desean ver. Esto ayudará a impulsar un mayor desarrollo del software con el tiempo.
- Ofrezca oportunidades de formación continua para las nuevas funciones, para que los usuarios se sientan seguros al utilizarlas una vez que se publiquen. Esto también garantizará que los clientes sepan cómo utilizar plenamente su inversión en su solución de desarrollo de software IVD.
Revolucionando la atención médica con el desarrollo de software IVD
El desarrollo de software de diagnóstico in vitro (IVD) ha transformado el sector sanitario al proporcionar soluciones rentables de pruebas, análisis, informes y comunicación sin equipos de laboratorio físicos.
Los estudios indican que los proveedores de atención médica dan alta prioridad a los procedimientos de diagnóstico in vitro (IVD), y su optimización tiene el potencial de mejorar los resultados de los pacientes. Por lo tanto, el desarrollo de software IVD es crucial para facilitar resultados de diagnóstico más rápidos y precisos, lo que en última instancia conduce a la optimización de las prácticas de atención médica.
Si necesita un socio en el desarrollo de software IVD para su negocio, MDx CRO es una consultoría de IVD que proporciona soluciones integrales para acompañarle en cada paso del proceso. Nuestro equipo de estrategas de CRO altamente experimentados tiene una amplia experiencia en llevar dispositivos médicos innovadores y tecnologías IVD al mercado. Solicite hoy mismo su consulta experta.
Preguntas frecuentes
¿Cuáles son las consideraciones clave al diseñar software IVD?
Hay varias consideraciones clave que las empresas deben tener en cuenta al diseñar software IVD: los requisitos del usuario, los requisitos reglamentarios según la ubicación geográfica de destino, la precisión de los datos y la gestión eficaz de los datos, la capacidad del software para integrarse con otros sistemas, así como el rendimiento y la usabilidad.
¿Cuáles son los requisitos reglamentarios para el desarrollo de software IVD en Europa?
Los requisitos reglamentarios para el desarrollo de software IVD en Europa están determinados por el Reglamento de diagnóstico in vitro (IVDR), que se hizo aplicable el 26 de mayo de 2022. Incluyen, entre otros, el diseño y el desarrollo, la gestión de riesgos, la validación y la verificación, así como el cumplimiento del RGPD.
¿Cuáles son los desafíos más comunes en el desarrollo de software IVD?
Los desafíos más comunes en el desarrollo de software IVD incluyen el cumplimiento normativo (que puede ser complejo y difícil de superar), garantizar la compatibilidad de la integración con otros sistemas, la gestión eficaz de los datos y una gran experiencia de usuario, entre otros.
¿Cómo se garantiza la calidad y la fiabilidad del software IVD?
Para garantizar la calidad y la fiabilidad del software IVD, es importante que las empresas sigan todas las directrices reglamentarias aplicables a su ubicación geográfica y utilicen un sistema de gestión de calidad para garantizar que el proceso de desarrollo esté bien documentado. La realización de pruebas, la validación y los procesos de verificación es otro elemento esencial del desarrollo de software para el diagnóstico in vitro.





