
El CRO MedTech que acelera tu acceso al mercado europeo
MDx nació con un propósito claro: ser el socio de referencia para fabricantes de dispositivos médicos e IVD que buscan navegar el entorno regulatorio europeo con rigor y agilidad. Hoy somos el equipo CRO especializado en MedTech más grande de la UE, con más de 40 profesionales, presencia en Barcelona, Madrid, Lisboa y Londres, y la confianza de los principales fabricantes globales del sector, incluyendo empresas del Top 10 mundial en IVD y Medical Devices.
El CRO MedTech especializado en IVD y Dispositivos Médicos
MDx es una organización de investigación por contrato (CRO) y consultoría regulatoria especializada en diagnóstico in vitro (IVD) y dispositivos médicos. Con sede en Barcelona, Madrid, Lisboa y Londres, y expertos activos en Europa, EE. UU. y APAC, acompañamos a fabricantes globales en los marcos regulatorios más exigentes: IVDR, MDR, ISO, MHRA, marcado CE y FDA.
Fundada por profesionales con trayectoria directa en organismos notificados e investigación clínica, MDx combina estrategia regulatoria de precisión con ejecución clínica rigurosa — desde el concepto inicial hasta el post-mercado.

Misión y visión
Misión
Visión
Qué hacemos
Asuntos regulatorios
Investigación clínica (servicios CRO)
Calidad y cumplimiento
Representación regulatoria
Formación
Nuestros valores
Resolvemos desafíos regulatorios complejos con soluciones prácticas y expertas.
Creemos en el éxito compartido a través de asociaciones sólidas y colaborativas.
El aprendizaje continuo y la mejora son fundamentales para nuestro servicio y nuestra gente.
Escalamos con nuestros clientes, desde empresas emergentes hasta líderes del mercado.
Diversos equipos impulsan mejores decisiones, innovación y resultados.
Carlos Galamba – CEO
Antiguo gerente técnico global de DIV y líder clínico en BSI, un organismo notificado líder y asesor de la Comisión Europea en asuntos regulatorios. Amplia experiencia en DIV de clase C/D, diagnósticos complementarios y generación de evidencia clínica.

David Tome – Presidente
Especialista en operaciones clínicas globales y estrategia regulatoria. Amplia experiencia en dispositivos médicos, diagnósticos y SaMD. Conocido por apoyar a los innovadores de MedTech a través de la ampliación y el diseño de ensayos.

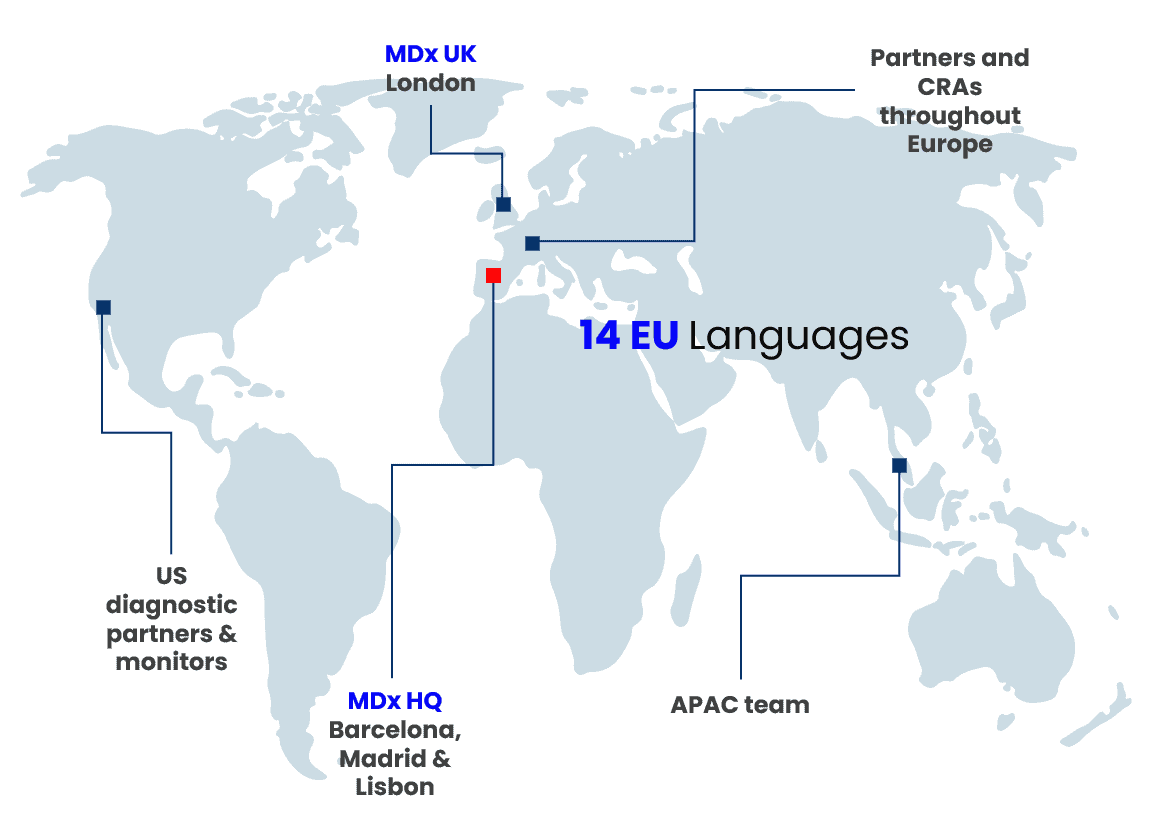
- Oficinas en Barcelona, Madrid, Lisboa y Londres
- Socios clínicos y regulatorios en UE, Reino Unido, EE. UU. y APAC
- Colaboradores con organismos notificados, asociaciones comerciales, plataforma de tecnología médica y farmacéutica (MPP) y más
- Hablamos 14 idiomas de la UE
- Representación en mercados globales clave
| Característica |
|---|
| Doble experiencia regulatoria + CRO |
| Enfoque en DIV y dispositivos |
| Representación + ejecución |
| Alcance regulatorio global |
| Ágil y escalable |
| Enlace con organismos notificados y autoridades |
| MDx CRO |
|---|

Trabaje con un socio que hable su idioma regulatorio.
MDx combina el conocimiento regulatorio experto con la excelencia clínica, lo que ayuda a los equipos de MedTech a tener éxito en cada etapa.
Precisión. Asociación. Rendimiento.


