
Su socio de precisión para diagnósticos complementarios y ensayos basados en biomarcadores
MDx CRO es una CRO de medicina de precisión y diagnósticos complementarios que ayuda a los equipos de IVD y farmacéuticos a diseñar y ejecutar estudios clínicos de CDx. Gestionamos el desarrollo de CDx desde la validación de biomarcadores hasta el cumplimiento del IVDR, las presentaciones Q de la FDA y la ejecución clínica conforme a la norma ISO 20916.
CRO de CDx servicio completo para medicina de precisión
MDx CRO es una CRO especializada en diagnósticos complementarios que ayuda a los equipos farmacéuticos y de IVD a planificar y ejecutar estudios clínicos de diagnósticos complementarios. Alineamos la estrategia de biomarcadores y la validación de ensayos con el Anexo XIV del IVDR y las vías de presentación PMA/Q de la FDA para acelerar el acceso al mercado en Europa (UE/Reino Unido) y en los EE. UU.
Desde la selección de la vía SRD frente a NSRD y la preparación de la presentación Q hasta el diseño y la monitorización del estudio ISO 20916, nuestro equipo ofrece una ejecución CRO de CDx integral, que incluye la delegación del patrocinador y los servicios de representante legal en la UE/Reino Unido.

Su viaje de diagnóstico complementario
Totalmente gestionado, paso a paso
UN OBJETIVO
Guiamos a los patrocinadores de medicina de precisión a través de cada fase crítica, alineando los flujos de trabajo clínicos, regulatorios y operativos para acelerar su camino hacia la aprobación.
Defina su vía de desarrollo con la orientación de expertos sobre los requisitos de la FDA y el IVDR, incluidas las determinaciones SRD frente a NSRD, las reuniones de presentación Q y las presentaciones PMA. Nuestra inteligencia regulatoria abarca los EE. UU. y la UE.
Soporte para el descubrimiento de biomarcadores, el desarrollo de ensayos clínicos, la validación analítica y la estrategia de biomarcadores traslacionales. Incluye la validación de ensayos para plataformas qPCR, NGS, IHC y SaMD.
Calificamos a los proveedores de laboratorio, LDT y centros de pruebas según los requisitos de la norma ISO 15189 y el marcado CE, realizando la diligencia debida para la idoneidad de las pruebas y el cumplimiento del IVDR para los ensayos clínicos destinados a las declaraciones CDx.
Desde la definición de CPSP y puntos finales hasta la gestión de riesgos y el consentimiento informado, diseñamos y ejecutamos ensayos clínicos conformes a la norma ISO 20916. MDx puede actuar como su representante legal en la UE/Reino Unido.
Operaciones clínicas integrales: calificación, formación, monitorización y preparación para auditorías del centro, lo que garantiza la adhesión al protocolo y la alineación con las BPC con la ISO 20916 en la monitorización in situ y remota.
Gestionamos el diseño de eCRF, el análisis estadístico y el desarrollo de informes de estudios de rendimiento clínico para las presentaciones del IVDR, incluidos los informes de estudios de rendimiento clínico para el Anexo XIV del IVDR.
Desde paquetes de presentación Q y PMA de la FDA; aplicaciones del Anexo XIV del IVDR, gestionamos todas las comunicaciones con las autoridades éticas y competentes, las RFI y las modificaciones.
Clasificación y respuesta de eventos adversos, incluidas las comunicaciones con el organismo notificado y el comité de ética. Cubre la notificación de seguridad del IVDR en los ensayos clínicos.
| Característica – capacidad |
|---|
| Soporte para las presentaciones del Anexo XIV del IVDR (CDx) |
| Consultoría de CDx (FDA + UE) |
| Monitorización ISO 20916 (CDx) |
| Delegación del patrocinador y representante legal en la UE/Reino Unido |
| Desarrollo de documentación de IVD |
| Experiencia traslacional y en biomarcadores |
| Inteligencia regulatoria |
| MDx CRO | Otras CRO | Equipos internos |
|---|---|---|
Áreas terapéuticas y tecnologías
Enfoque terapéutico
Tecnologías y plataformas
Aplicaciones de biomarcadores

A quién servimos
- Empresas farmacéuticas globales que codesarrollan diagnósticos complementarios
- Fabricantes de IVD y CDx
- Desarrolladores de diagnósticos centrados en la oncología
- Patrocinadores con sede en EE. UU. que realizan estudios clínicos de diagnósticos complementarios en Europa
- Plataformas de software y diagnóstico digital

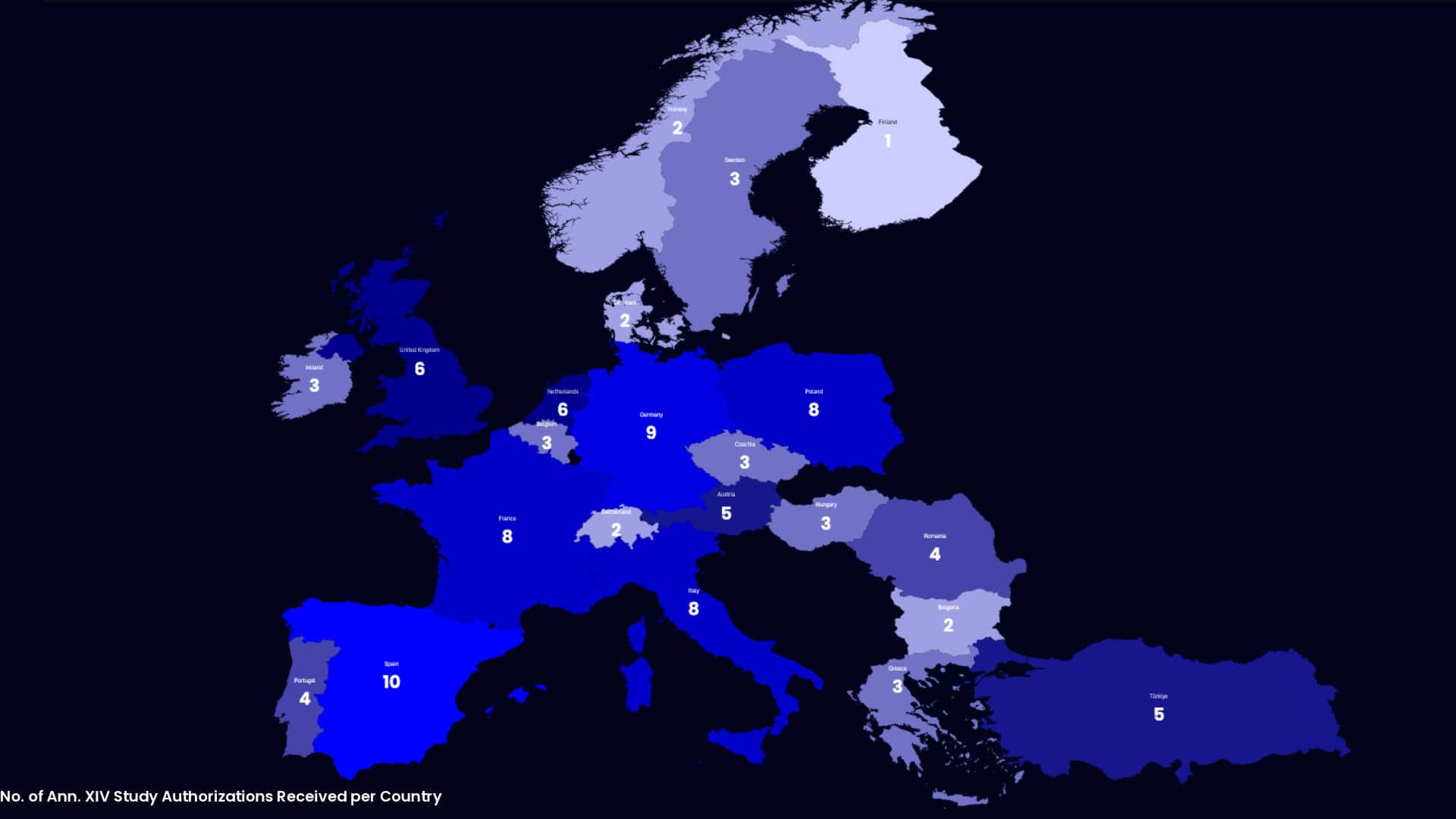
Programas comerciales de CDx entregados
MDx ha apoyado con éxito la ejecución de estudios de rendimiento y las presentaciones regulatorias para programas de CDx comercializados en todo el mundo.
Apoyamos los diagnósticos complementarios desde la validación clínica hasta la presentación Q/PMA de la FDA y las aplicaciones del Anexo XIV del IVDR, alineando los plazos de CDx con el desarrollo de fármacos, incluidas las consultas con la EMA y el organismo notificado.
Nuestro historial incluye:
- Ensayos IHC HER2 para cáncer de mama y gástrico
- Kits de detección de mutaciones EGFR para CPNM
- Paneles NGS con declaraciones de CDx (CCR y tumores sólidos)
- Ensayos multiplex y qPCR validados según IVDR y FDA
Preguntas frecuentes
Haga una pregunta-
¿Qué es la decisión SRD frente a NSRD para CDx en los EE. UU.?
La FDA distingue entre estudios de dispositivo de riesgo significativo (SRD) y de dispositivo de riesgo no significativo (NSRD). Guiamos a los patrocinadores de CDx a través de las interacciones de la presentación Q y determinamos el camino correcto hacia la PMA u otras presentaciones.
-
¿Qué es el Anexo XIV del IVDR para los diagnósticos complementarios?
El Anexo XIV define los requisitos del estudio de rendimiento clínico para los IVD, incluidos los CDx, en la UE. Cubre las presentaciones, los procesos éticos/de la autoridad competente y las expectativas de evidencia para la evaluación de la conformidad del IVDR.
-
¿Puede MDx actuar como representante legal para los estudios de rendimiento de CDx e IVDR en la UE?
Sí. Ofrecemos servicios de patrocinador delegados, presentaciones a autoridades éticas/competentes y representación legal, gestionando la documentación y las comunicaciones en su nombre.
-
¿Apoyan tanto el IVDR como la presentación Q o PMA de la FDA para CDx?
Absolutamente. Definimos estrategias de presentación, coordinamos la generación de evidencia y gestionamos las comunicaciones integrales con los organismos notificados de la UE, la EMA y la FDA, incluidas las presentaciones Q/PMA de la FDA y las aplicaciones del Anexo XIV del IVDR.
-
¿Qué desafíos existen al ejecutar estudios combinados bajo el CTR y el IVDR?
Los estudios combinados se enfrentan a una desalineación regulatoria: el IVDR y el CTR tienen diferentes requisitos, plazos y vías de presentación. MDx ayuda a los patrocinadores a navegar por estas complejidades mediante el desarrollo de estrategias integradas, asegurando que tanto los datos clínicos como los de rendimiento cumplan con las distintas expectativas de los reguladores de productos sanitarios y medicamentos.

Aceleremos su CDx al mercado
Tanto si está codesarrollando un CDx con un socio farmacéutico como si está preparando su primera presentación del Anexo XIV del IVDR, MDx es su CRO de diagnósticos complementarios de servicio completo para el éxito regulatorio y la aprobación global, ofreciendo estudios ISO 20916, representante legal en la UE/Reino Unido y soporte para la presentación Q/PMA de la FDA.
Su CDx. Nuestra experiencia. Impacto global.

