La usabilidad de los dispositivos médicos no es solo una cuestión de comodidad. Es una cuestión de seguridad, eficacia y cumplimiento normativo. Un diseño deficiente que confunde o frustra a los usuarios puede provocar errores de uso, efectos adversos e incluso daños al paciente. Para abordar esto, la norma internacional IEC 62366-1:2015/Amd 1:2020 establece un marco estructurado para la ingeniería de la usabilidad en el desarrollo de dispositivos médicos.
Para los fabricantes de dispositivos médicos, es esencial comprender y aplicar la norma IEC 62366. El cumplimiento demuestra que los riesgos de usabilidad se han identificado, reducido y documentado, lo cual es esencial para todos los dispositivos médicos , incluidos los DIV y el Software como dispositivo médico (SaMD) .
¿Qué es la norma IEC 62366?
La norma IEC 62366 es la norma reconocida internacionalmente que define cómo integrar la usabilidad en el proceso de diseño y desarrollo.
Tiene dos partes principales:
- IEC 62366-1:2015/Amd 1:2020 Dispositivos médicos – Aplicación de la ingeniería de la usabilidad a los dispositivos médicos: La norma principal que describe el proceso de ingeniería de la usabilidad.
- IEC/TR 62366-2:2016 Dispositivos médicos – Guía sobre la aplicación de la ingeniería de la usabilidad a los dispositivos médicos: Un informe técnico que proporciona orientación y ejemplos para apoyar la implementación.
El objetivo es garantizar que la ingeniería de la usabilidad se aplique de manera coherente para que los dispositivos puedan ser utilizados de forma segura y eficaz por los usuarios previstos, en los entornos de uso previstos, al tiempo que se garantiza que los errores de uso que podrían causar daños se identifiquen, reduzcan y controlen mediante actividades de usabilidad estructuradas.
Por qué es importante la ingeniería de la usabilidad
Los errores relacionados con el uso son una de las principales causas de efectos adversos relacionados con los dispositivos. Al integrar la ingeniería de la usabilidad en el desarrollo de productos, los fabricantes pueden:
- Reducir los errores de uso que podrían causar daños
- Mejorar la seguridad del paciente y los resultados del tratamiento
- Satisfacer los requisitos reglamentarios de MDR, IVDR y la FDA
- Aumentar la aceptación del usuario y el éxito en el mercado
- Reducir los costes a largo plazo evitando rediseños o retiradas
En resumen, la usabilidad es tanto un requisito de cumplimiento como una ventaja competitiva.
Guía paso a paso para aplicar la norma IEC 62366
The usability engineering process defined in IEC 62366 is systematic and iterative. It integrates into the overall product development lifecycle and risk management process in line with ISO 14971. Below is a step-by-step breakdown.
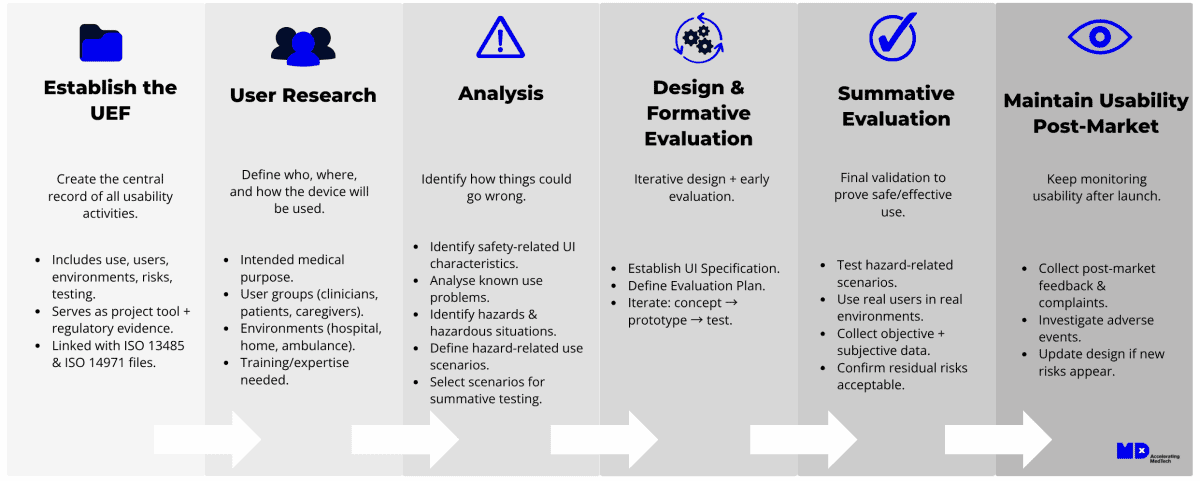
1. Establecer el archivo de ingeniería de la usabilidad (UEF)
El UEF es el repositorio central de documentación para todas las actividades de usabilidad. Incluye el uso previsto, los perfiles de usuario, los escenarios de uso, el análisis de riesgos, los resultados de las pruebas y las medidas de control de riesgos. En la práctica, los registros y otros documentos que forman el UEF también pueden formar parte del archivo de diseño del producto (ISO 13485) o del archivo de gestión de riesgos (ISO 14971).
Piense en el UEF como una herramienta de gestión de proyectos y como prueba para los reguladores.
2. Investigación de usuarios
Prepare la Especificación de uso. Aquí es donde se define:
- El propósito médico previsto del dispositivo
- Los grupos de usuarios (por ejemplo, médicos, pacientes, legos, cuidadores)
- Los entornos de uso (hospitales, hogares, ambulancias, clínicas)
- Cualquier formación o experiencia requerida
Esto constituye la base de todas las actividades de usabilidad posteriores.
3. Análisis
Una vez que sepa quién va a utilizar su dispositivo y dónde, el siguiente paso es analizar cómo podrían salir mal las cosas.
Las actividades incluyen:
- Identificar las características de la interfaz de usuario relacionadas con la seguridad (por ejemplo, la legibilidad de las pantallas, la disposición de los botones, la visibilidad de las alarmas).
- Revisar los datos posteriores a la producción y las bases de datos públicas para detectar problemas de usabilidad conocidos con dispositivos similares.
- Identificar los peligros y las situaciones peligrosas.
- Identificar y describir los escenarios de uso relacionados con los peligros, que describen exactamente cómo podrían producirse errores de uso y qué consecuencias podrían tener.
- Seleccionar escenarios de uso relacionados con los peligros para la evaluación sumativa.
Estos escenarios se priorizan para decidir cuáles se evaluarán en las pruebas sumativas.
4. Diseño y evaluación formativa
Aquí es donde el diseño y las pruebas de usabilidad se realizan en ciclos iterativos.
Pasos clave:
- Establecer la especificación de la interfaz de usuario: el plano de todos los elementos de la interfaz de usuario.
- Desarrollar el plan de evaluación de la interfaz de usuario: definir cómo se realizarán las pruebas formativas y sumativas.
- Ciclos iterativos de concepto, prototipo y pruebas
El objetivo de la evaluación formativa es encontrar problemas de usabilidad de forma temprana, antes de la validación final, para que los cambios sean más baratos y menos disruptivos.
5. Evaluación sumativa
La etapa final es una validación sumativa de la usabilidad. Se trata de una prueba formal que demuestra a los reguladores que el dispositivo puede ser utilizado de forma segura y eficaz por los usuarios previstos.
- Probar los escenarios de uso relacionados con los peligros identificados anteriormente.
- Utilizar usuarios representativos en entornos realistas.
- Recopilar datos objetivos de rendimiento (finalización de tareas, tasas de error) y comentarios subjetivos (facilidad de uso, confianza).
- Confirmar que los riesgos residuales son aceptables de acuerdo con la norma ISO 14971.
Esta etapa proporciona la evidencia objetiva que los reguladores requieren para garantizar el cumplimiento.
6. Mantener la usabilidad después de la comercialización
La ingeniería de la usabilidad no termina con el lanzamiento del producto. La vigilancia posterior a la comercialización debe recopilar comentarios sobre problemas de usabilidad, efectos adversos y reclamaciones. Es posible que se requieran actualizaciones o cambios de diseño si surgen nuevos riesgos.
Retos comunes en la aplicación de la norma IEC 62366
Muchos fabricantes se encuentran con dificultades como:
- Subestimar los recursos necesarios para las pruebas de usabilidad
- Reclutar usuarios representativos para estudios formativos y de validación
- Definir escenarios de uso realistas que reflejen los entornos clínicos reales
- Integrar la usabilidad con los plazos de desarrollo
- Documentar correctamente las pruebas en el UEF
No abordar estos retos puede resultar en el rechazo reglamentario, retrasos o rediseños costosos.
Buenas prácticas para el éxito
- Comenzar la ingeniería de la usabilidad pronto en el proceso de diseño
- Involucrar a equipos multidisciplinares que incluyan ingenieros, médicos y expertos en usabilidad
- Utilizar una mezcla de métodos cualitativos y cuantitativos en las evaluaciones
- Priorizar los escenarios de uso relacionados con los peligros en las pruebas de validación
- Documentar todo a fondo en el archivo de ingeniería de la usabilidad
- Siempre que sea posible, involucrar a los reguladores pronto para la alineación
- Aprovechar la experiencia especializada, como la de una consultoría de dispositivos médicos y DIV con experiencia en ingeniería de la usabilidad
Preguntas frecuentes
Yes. The latest versions of the IEC 62366 standards are recognised by the FDA as consensus standards. However, the FDA has also published specific human factors engineering guidances with minor differences to IEC 62366 so it is recommended that these are also considered for FDA submissions.
Throughout development. Formative evaluations identify and correct issues early, while summative validation confirms safe and effective use before market approval.
Yes, provided they are representative of real-world conditions and cover all critical tasks and hazard-related use scenarios.
EC 62366-1 is the main normative standard that defines the usability engineering process manufacturers must follow. IEC 62366-2 is a companion informative document that provides guidance and rationale to help apply IEC 62366-1 in practice. For regulatory submissions, compliance with IEC 62366-1 is what notified bodies and regulators assess — IEC 62366-2 is a supporting resource, not a requirement.
The Usability Engineering File (UEF) is the core documentation output of the IEC 62366-1 process. It must document the intended use and user groups, use scenarios and user interface specification, formative evaluation records, summative evaluation plan and results, and risk-related findings and how they were addressed. It should be structured to allow a notified body or regulatory reviewer to trace the full usability engineering process from start to finish.
Yes. IEC 62366-1 applies to all medical devices, including in vitro diagnostic devices (IVDs). Under the EU IVDR and MDR, manufacturers are expected to demonstrate that human factors and usability have been considered as part of the design and development process. This is particularly relevant for IVDs used at the point of care or by lay users, where use errors can have direct patient safety implications.
There is no fixed number mandated by IEC 62366-1, but common practice — and FDA guidance — typically expects a minimum of 15 participants per user group for summative evaluations. The number should be justified based on the diversity of the user population, the complexity of the device, and the number of critical tasks being evaluated. For high-risk devices or large user populations, a larger sample may be required.
Formative evaluations are iterative assessments carried out during device development to identify and resolve usability problems early. They are exploratory in nature and do not need to meet a pre-defined pass/fail criterion. Summative evaluations, also called validation testing, are conducted on a near-final or final version of the device to confirm that users can operate it safely and effectively without being coached or corrected. Summative results are what get submitted to regulators.
Cómo puede ayudar MDx CRO
La implementación interna de la norma IEC 62366 puede sobrecargar los recursos. En MDx CRO podemos proporcionar:
- Desarrollo de protocolos y diseño de estudios para pruebas de usabilidad
- Reclutamiento de usuarios representativos en todas las geografías
- Moderación de estudios formativos y de validación
- Integración de la ingeniería de la usabilidad con la estrategia reguladora
- Preparación de toda la documentación de usabilidad necesaria para las presentaciones, incluidas las presentaciones a la FDA
Como consultoría de confianza en dispositivos médicos y DIV, apoyamos a los fabricantes en la implementación de la norma IEC 62366, la realización de estudios de usabilidad y la preparación de documentación que satisfaga a los reguladores de la UE y de EE. UU. Tanto si está iniciando un nuevo proyecto como si está actualizando un dispositivo existente, nuestro equipo le ayuda a lograr el cumplimiento y a ofrecer dispositivos más seguros al mercado.
Need help with IEC 62366 compliance?
Talk to our usability engineering team.






