El International Medical Device Regulators Forum (IMDRF) ha publicado un nuevo borrador de guía de gran calado: IMDRF/CEIVD WG/N91: Clinical Evidence for IVD Medical Devices, Definitions and Principles of Performance Evaluation, abierto a consulta pública del 4 de marzo al 5 de mayo de 2026. Para los fabricantes de IVD, equipos de asuntos regulatorios y desarrolladores de diagnósticos companion (CDx), no se trata de una actualización menor, sino de una reformulación integral del marco de referencia global sobre cómo se define, genera, documenta y defiende la evidencia clínica.
Este artículo analiza qué cambia realmente con el N91, qué implica para los distintos tipos de fabricantes y, basado en la experiencia de Carlos Galamba apoyando presentaciones IVDR y programas CDx en MDx CRO, qué pasos prácticos deberían adoptarse ahora.
¿Por qué importa ahora?
La consulta del IMDRF abrió el 4 de marzo de 2026 y se cierra el 5 de mayo de 2026. Los fabricantes con productos en desarrollo, portfolios legacy en revisión, programas CDx en curso o IVD basados en IA en cualquier fase deberían leer este borrador detenidamente y considerar el envío de comentarios antes de la fecha límite.
IMDRF N91: una reformulación del marco, no una simple revisión
IMDRF N91 es un borrador de guía elaborado por el Grupo de Trabajo de Evidencia Clínica para IVD del IMDRF. Su título completo es Clinical Evidence for IVD Medical Devices, Definitions and Principles of Performance Evaluation, y representa la actualización más significativa del marco global de evidencia clínica para IVD desde que se publicaron los documentos originales del GHTF.
El documento tiene 31 páginas e introduce 17 términos definidos, consolidando un vocabulario que históricamente ha sido inconsistente entre jurisdicciones. Establece un modelo de evidencia basado en el ciclo de vida que va más allá de la generación de evidencia precomercialización y vincula explícitamente la evaluación del rendimiento con la finalidad prevista, el estado del arte y las actualizaciones postcomercialización.
Qué documentos sustituye
IMDRF N91 reemplaza ambos documentos:
- GHTF/SG5/N6:2012 – Scientific Validity Determination and Performance Studies for IVD Medical Devices
- GHTF/SG5/N7:2012 – Key Definitions and Concepts
Estos dos documentos han sido el punto de referencia global para la evidencia clínica de IVD desde 2012. Su sustitución por un único marco actualizado supone una consolidación relevante.
El papel del IMDRF en el panorama regulatorio
El IMDRF no es un órgano legislativo. Sus documentos de guía no son jurídicamente vinculantes. Sin embargo, tienen un peso significativo porque son desarrollados por las agencias reguladoras de los principales mercados: la Comisión Europea, la FDA, Health Canada, la TGA (Australia), la PMDA (Japón) y otras. Los documentos del MDCG (que gobiernan la interpretación del IVDR en la UE) hacen referencia explícita a conceptos del IMDRF, y los revisores regulatorios de Organismos Notificados y autoridades competentes utilizan de forma habitual los marcos del IMDRF como referencia.
En la práctica, esto significa que una vez que una guía del IMDRF se finaliza, los fabricantes que no estén alineados se enfrentarán cada vez más a preguntas durante las revisiones técnicas, auditorías y presentaciones, incluso si la guía no se cita formalmente como requisito legal.
«En mi experiencia, los equipos regulatorios serios empiezan a alinearse casi de inmediato, incluso antes de que la referencia formal se convierta en rutina. La incorporación activa en plantillas de revisión, formación y lenguaje de auditoría suele tardar entre 6 y 18 meses, dependiendo de la jurisdicción y la organización. Mi consejo es no esperar a un lenguaje de enforcement formal: si la dirección es clara, empieza a alinear tu estrategia de evidencia ahora.»
Carlos Galamba, CEO de MDx
Los tres pilares de la evidencia clínica según IMDRF N91
N91 formaliza y se alinea con la estructura de tres pilares ya integrada en el IVDR de la UE: validez científica, rendimiento analítico y rendimiento clínico. Juntos constituyen la evidencia clínica que los fabricantes deben generar, documentar y mantener a lo largo del ciclo de vida del dispositivo.
Validez científica: establecer la asociación del biomarcador
La validez científica aborda si el analito medido está genuinamente asociado con la condición clínica o el estado fisiológico que el dispositivo pretende detectar. Para muchos biomarcadores establecidos, esto es esencialmente un ejercicio basado en la literatura. Para biomarcadores novedosos, es una tarea de investigación sustancial que debe comenzar mucho antes de lo que la mayoría de los equipos esperan.
«En el contexto de CDx, este trabajo debería comenzar tan pronto como la selección del biomarcador y la definición de la finalidad prevista. Bajo el IVDR, el plan de evaluación del rendimiento debe mapear las fases de desarrollo y la secuencia para establecer validez científica, rendimiento analítico y rendimiento clínico, de modo que este trabajo realmente comienza en la fase traslacional, no en la fase de presentación.»
Carlos Galamba
N91 deja claro que la validez científica no puede asumirse. Debe documentarse, y para analitos novedosos sin consenso clínico establecido, la ausencia de validez científica bloqueará toda la vía de evidencia.
Rendimiento analítico: lo que los fabricantes de IVD subestiman con mayor frecuencia
El rendimiento analítico abarca la capacidad del dispositivo para detectar o medir el analito con precisión y fiabilidad, incluyendo precisión, reproducibilidad, justificación de puntos de corte, estabilidad de la muestra, factores preanalíticos, interferencias y comparabilidad.
«Cuando se trabaja con ensayos de ensayos clínicos o CDx, los equipos suelen estar muy centrados en la historia del biomarcador y el programa del fármaco, por lo que asumen que el ensayo puede optimizarse más adelante. En realidad, los reguladores a menudo examinan primero la robustez analítica. El IVDR ya exige a los fabricantes construir el caso de evidencia en los tres pilares, no solo en el rendimiento clínico.»
Carlos Galamba
Este es un patrón que MDx CRO encuentra regularmente, especialmente en programas CDx donde la hipótesis clínica está bien desarrollada pero el paquete analítico se trata como algo secundario. N91 refuerza que los reguladores, incluidos los Organismos Notificados y la FDA, evaluarán el rendimiento analítico en profundidad, no simplemente lo aceptarán como una formalidad técnica.
Rendimiento clínico: qué documentación se requiere frente a qué evidencia debe generarse
El rendimiento clínico se refiere a la capacidad del dispositivo para producir resultados que se correlacionen con una condición clínica en la población diana prevista. N91 aclara una distinción importante con implicaciones operativas significativas: los fabricantes siempre deben documentar el rendimiento clínico, pero no siempre necesitan generar nueva evidencia mediante un estudio prospectivo.
La necesidad de nueva evidencia depende de la clase de riesgo del dispositivo, la novedad del analito, la población de uso previsto y los datos publicados disponibles. Esto refleja el marco del IVDR, donde la literatura existente, los datos de registros y las experiencias publicadas de uso diagnóstico rutinario pueden contribuir a la base de evidencia de rendimiento clínico, si son suficientes y metodológicamente sólidas.
Para obtener más información sobre cómo se diseñan y llevan a cabo los estudios de rendimiento clínico en el marco del IVDR, consulte nuestra guía: «Realización de estudios clínicos en el marco del IVDR: lo que necesita saber».
Software como IVD (SaIVD) e IA/ML: qué cambia con IMDRF N91
Una de las adiciones más sustantivas del N91 es su sección dedicada al Software como IVD (SaIVD), incluyendo los IVD que incorporan inteligencia artificial y aprendizaje automático. Esto refleja una brecha regulatoria real: los documentos GHTF de 2012 eran anteriores al despliegue generalizado de diagnósticos basados en IA, y los fabricantes han estado operando sin un marco global claro sobre qué aspecto debe tener la evidencia clínica para estos productos.
N91 requiere que los fabricantes de SaIVD basados en IA aborden: la trazabilidad del ciclo de vida de los datos, la monitorización de la deriva del rendimiento, la transparencia de las salidas de IA y la documentación del punto de transición en el que las recomendaciones de IA son revisadas por profesionales sanitarios cualificados. De forma crítica, N91 afirma que las decisiones clínicas finales deben recaer siempre en profesionales sanitarios cualificados, no en el sistema de IA en sí.
El error más común en los paquetes de evidencia de IVD basados en IA
«El error más común es tratar la precisión del algoritmo como si fuera por sí sola evidencia clínica. Para los IVD basados en IA, también se necesita demostrar la procedencia de los datos, la representatividad, el control de versiones, el rendimiento en escenarios de entrada del mundo real, la monitorización de la deriva y la transparencia sobre las limitaciones. El borrador del IMDRF es bastante claro en que para los SaIVD basados en IA, los fabricantes deben documentar todo el ciclo de vida de los datos, gestionar los modos de fallo específicos de la IA, monitorizar la deriva postcomercialización y hacer que las salidas sean lo suficientemente interpretables para la supervisión humana.»
Carlos Galamba
Esta es una brecha operativa significativa para muchas empresas de software e IA que entran en el espacio IVD. Las métricas de rendimiento del algoritmo (sensibilidad, especificidad, AUC) son necesarias pero no suficientes. N91 indica que los reguladores esperarán una arquitectura de evidencia mucho más amplia para estos productos.
Para más información sobre el enfoque de la IMDRF respecto a la inteligencia artificial en los productos sanitarios, véase: «Productos sanitarios basados en el aprendizaje automático de la IMDRF: términos y definiciones clave».
IMDRF N91 y diagnósticos companion: co-desarrollo, fijación de puntos de corte y estudios de bridging clínico
Los diagnósticos companion (CDx) reciben un tratamiento dedicado y sustancialmente más detallado en N91 que en los documentos GHTF de 2012. Esto refleja tanto la creciente complejidad regulatoria de los programas CDx a nivel global como los desafíos específicos que surgen cuando un IVD debe ser co-desarrollado junto con, y validado en el contexto de, un ensayo clínico terapéutico.
N91 aborda explícitamente la relación entre el CDx y su programa de fármaco vinculado, incluyendo consideraciones de diseño del ensayo clínico (estratificación terapéutica vs. selección terapéutica), el papel del diagnóstico companion en la definición de la población elegible de pacientes y el uso de estudios de bridging para establecer la comparabilidad entre un ensayo de ensayo clínico y el CDx comercial final.
El mayor desafío práctico en el desarrollo de CDx: la alineación de cronogramas
«La parte más difícil suele ser fijar el ensayo y su punto de corte lo suficientemente pronto para el ensayo del fármaco, mientras se deja margen para evolucionar hacia el CDx comercial final. En la práctica, los equipos quieren flexibilidad durante el desarrollo clínico temprano, pero los reguladores quieren trazabilidad, reproducibilidad y un puente defendible hacia el dispositivo final. Esa tensión es lo que hace que los programas CDx sean operativamente difíciles.»
Carlos Galamba
Estudios de bridging clínico: donde los paquetes de evidencia fallan
Cuando se requiere un estudio de bridging, que vincula un ensayo de ensayo clínico con un CDx comercial posterior, los fabricantes frecuentemente llegan a la presentación con paquetes incompletos.
Las carencias comunes son una comparabilidad analítica débil, una justificación insuficiente de la transferencia de puntos de corte, una representatividad de muestras inadecuada y una explicación incompleta de los resultados discordantes. IMDRF N91 ahora reconoce directamente el bridging desde un ensayo de ensayo clínico hacia un CDx posterior y establece que el estudio debe demostrar la comparabilidad clínica utilizando datos directos o indirectos.»
Carlos Galamba
El reconocimiento explícito del bridging en N91 es significativo porque proporciona a los equipos regulatorios un marco definido al que hacer referencia y establece expectativas que los reguladores de las jurisdicciones miembros del IMDRF aplicarán cada vez más.
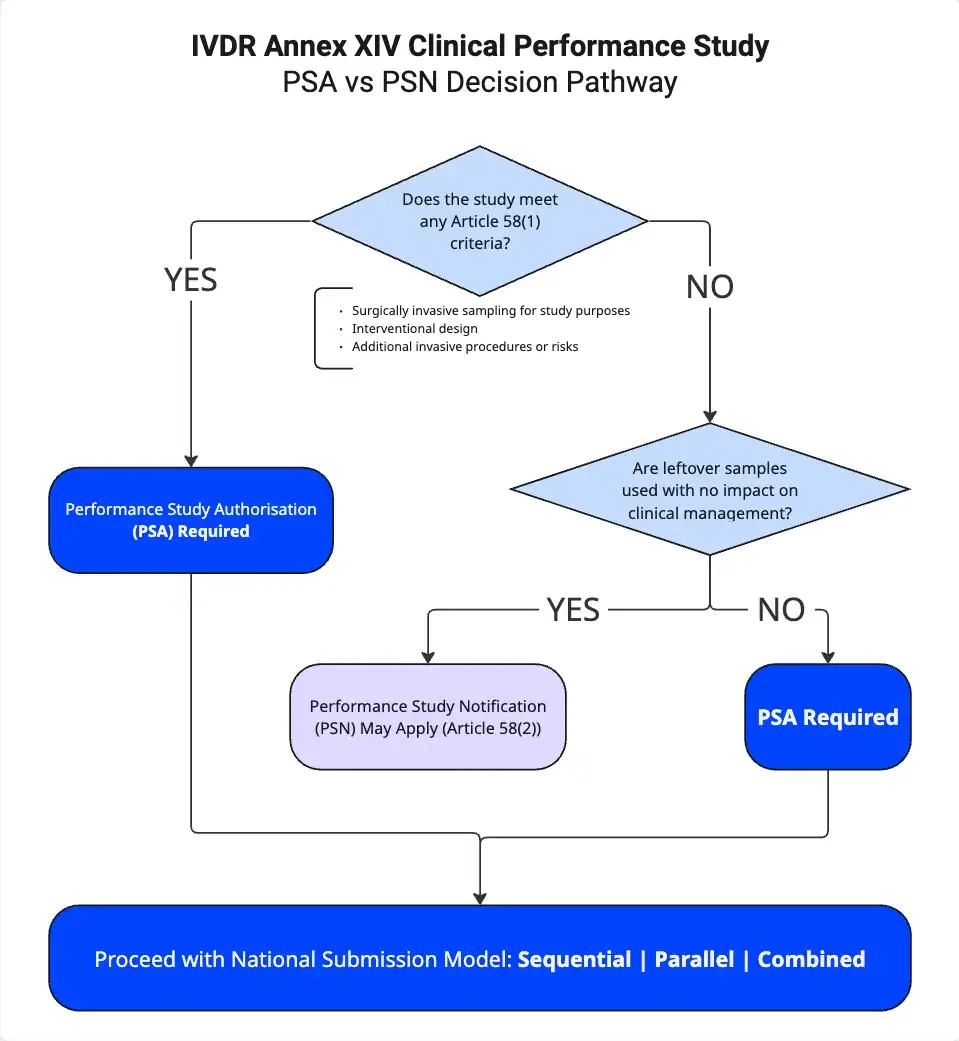
Para consultar una guía paso a paso sobre los estudios de rendimiento de los diagnósticos complementarios (CDx) en el marco del IVDR, véase: «Estudios de rendimiento de los diagnósticos complementarios según el anexo XIV del IVDR: una guía paso a paso 2026».
IMDRF N91 vs. IVDR: ¿qué cambia para los fabricantes que ya cumplen con la UE?
Una pregunta práctica para los fabricantes que ya operan bajo el IVDR: ¿requiere N91 un trabajo adicional significativo?
«Para un fabricante que cumple genuinamente con el IVDR, N91 no debería parecer una reinvención. El IVDR ya exige evidencia clínica basada en validez científica, rendimiento analítico y rendimiento clínico, respaldada por un proceso de evaluación del rendimiento continuo vinculado a la finalidad prevista y actualizado a lo largo del ciclo de vida. El trabajo adicional está principalmente en ajustar la estructura, la terminología y la justificación, especialmente para software, IA y CDx.»
Carlos Galamba
La frase clave es «cumple genuinamente con el IVDR». Muchos fabricantes tienen documentación que está técnicamente completa pero no lógicamente estructurada en torno a la finalidad prevista, el beneficio clínico y las actualizaciones de evidencia del ciclo de vida, los elementos que N91 hace más centrales.
Para conocer los requisitos específicos en materia de evidencia clínica del Reglamento sobre productos sanitarios para diagnóstico in vitro (IVDR), consulte: Requisitos de evidencia clínica del IVDR de MedTech Europe
Dónde puede requerirse trabajo adicional
| Área | Trabajo adicional probable para fabricantes conformes con IVDR |
|---|---|
| SaIVD / IVD basados en IA | N91 añade especificidad en documentación del ciclo de vida de datos, protocolos de monitorización de deriva y requisitos de transparencia que pueden exceder el alcance actual del expediente técnico IVDR. |
| Diagnósticos companion | La documentación de estudios de bridging y la justificación de transferencia de puntos de corte pueden necesitar estructurarse más formalmente según los requisitos de N91. |
| Portfolios legacy | Los paquetes de evidencia técnicamente completos pero no estructurados lógicamente en torno a la finalidad prevista y el beneficio clínico pueden necesitar reestructuración. |
| Alineación terminológica | N91 introduce 17 términos definidos. Asegurar que la documentación interna utilice terminología coherente y alineada con N91 reducirá la fricción con los revisores. |
¿Quién está más expuesto ante IMDRF N91?
«Los más expuestos son probablemente los titulares de portfolios legacy y los desarrolladores de IVD de IA/software. Los fabricantes legacy suelen tener paquetes de evidencia que están técnicamente completos pero no estructurados lógicamente en torno a la finalidad prevista, el beneficio clínico y las actualizaciones del ciclo de vida. Las empresas de IA y software se enfrentan a una complejidad adicional porque N91 aborda explícitamente el ciclo de vida de los datos, la deriva, la transparencia y la necesidad de re-verificación continua. Los desarrolladores de CDx también están altamente expuestos por los desafíos adicionales de bridging y co-desarrollo.»
Carlos Galamba
Las startups que construyen nuevos productos desde cero se enfrentan, en principio, a menos disrupciones: si diseñan su estrategia de evidencia en torno a N91 desde el primer día, están construyendo hacia el estándar en lugar de tener que adaptarse retroactivamente.
3 acciones a tomar antes de que cierre la consulta del IMDRF el 5 de mayo de 2026
N91 es inequívoco: la evidencia clínica es una actividad del ciclo de vida, no un entregable de precomercialización. Si la estrategia de evidencia de tu organización sigue organizada en torno a hitos de presentación en lugar de una evaluación del rendimiento continua y la disciplina de la finalidad prevista, este es el momento de cambiarlo.
- Realiza una evaluación de brechas estructurada
Mapea tus finalidades previstas actuales, informes de evaluación del rendimiento y planes de generación de evidencia contra el borrador N91. Céntrate específicamente en: cómo está documentada tu evidencia de los tres pilares y si está genuinamente vinculada a la finalidad prevista; si tus productos SaIVD o IA tienen documentación del ciclo de vida de datos y monitorización de deriva; y si tu evidencia de bridging CDx está estructurada de forma que satisfaga los requisitos de comparabilidad de la Sección 7 de N91.
- Identifica fricciones operativas y envía comentarios
La consulta pública es una oportunidad genuina para influir en la guía final. Los fabricantes deben identificar dónde N91 crea fricción operativa para sus tipos específicos de producto, particularmente en CDx, IA/software, NGS, testing descentralizado o portfolios legacy, y enviar comentarios concretos y técnicamente fundamentados al IMDRF antes del 5 de mayo de 2026.
- Audita tu mentalidad de evidencia
N91 es inequívoco: la evidencia clínica es una actividad del ciclo de vida, no un entregable de precomercialización. Si la estrategia de evidencia de tu organización sigue organizada en torno a hitos de presentación en lugar de una evaluación del rendimiento continua y la disciplina de la finalidad prevista, este es el momento de cambiarlo.
El periodo de consulta cierra el 5 de mayo de 2026. Los comentarios pueden enviarse a través de la página de consulta del IMDRF.
Si su equipo necesita ayuda para llevar a cabo una evaluación estructurada de las deficiencias o preparar una revisión técnica previa a la presentación, el servicio de evaluación previa a la presentación del IVDR de MDx CRO está diseñado precisamente para este tipo de tareas.
Cómo puede ayudar MDx
MDx CRO combina más de 18 años de experiencia regulatoria en IVD con experiencia práctica en Organismos Notificados, roles de asesoría de la Comisión Europea y liderazgo operativo en IVD Clase C/D, CDx, NGS y software diagnóstico basado en IA. Nuestro equipo ha apoyado cientos de presentaciones IVDR y continúa siguiendo los desarrollos regulatorios globales, incluyendo las consultas del IMDRF, en tiempo real.
Ya estés realizando una evaluación de brechas contra el borrador N91, construyendo tu estrategia de evidencia CDx, preparándote para una presentación IVDR o desarrollando un plan de evidencia clínica para un IVD basado en IA, nuestro equipo puede proporcionar la profundidad regulatoria y la experiencia operativa para avanzar de manera eficiente.
¿Listo para alinearte con IMDRF N91?
Contacta con MDx CRO para una evaluación de brechas estructurada contra el borrador N91 o para revisar tu estrategia de evidencia clínica actual antes de que la consulta cierre el 5 de mayo de 2026.
Preguntas frecuentes sobre IMDRF N91
IMDRF N91 es el borrador de 2026 del documento «Clinical Evidence for IVD Medical Devices, Definitions and Principles of Performance Evaluation». Abierto a consulta pública del 4 de marzo al 5 de mayo de 2026, sustituye los documentos GHTF N6 y N7 de 2012. Importa porque actualiza el marco de referencia global sobre cómo los fabricantes deben definir, generar, documentar y defender la evidencia clínica de IVD, incluyendo áreas modernas como software, IA y diagnósticos companion.
No. El IVDR 2017/746 de la UE sigue siendo el marco jurídicamente vinculante en la UE. IMDRF N91 se entiende mejor como un documento de guía de convergencia global altamente relevante para el IVDR porque la arquitectura central ya está alineada: finalidad prevista, validez científica, rendimiento analítico, rendimiento clínico, actualización del ciclo de vida y estado del arte.
Validez científica (establecer la asociación entre el analito y una condición clínica), rendimiento analítico (la capacidad del IVD para detectar o medir correctamente el analito) y rendimiento clínico (la capacidad del IVD para producir resultados que se correlacionen con una condición clínica en la población diana). Los tres deben abordarse en una estrategia de evaluación del rendimiento integrada vinculada a la finalidad prevista del dispositivo.
Sí. N91 incluye una sección dedicada al Software como IVD (SaIVD) que aborda explícitamente los dispositivos basados en IA y aprendizaje automático. Los requisitos incluyen documentación del ciclo de vida de datos, monitorización de la deriva del rendimiento, transparencia de la IA, control de versiones y el principio de que las decisiones clínicas finales deben recaer en profesionales sanitarios cualificados.
Un estudio de bridging clínico se utiliza para vincular un nuevo CDx comercial con un ensayo de ensayo clínico existente que se utilizó durante el estudio pivotal de un fármaco. N91 reconoce formalmente este enfoque y exige que los estudios de bridging establezcan la comparabilidad clínica utilizando datos de comparabilidad directa o indirecta. Esto aborda una brecha significativa en el marco regulatorio existente para el desarrollo de CDx.
N91 está actualmente en consulta pública, que cierra el 5 de mayo de 2026. La guía se finalizará después de revisar los comentarios. Actualmente no está en vigor, pero los fabricantes que se alineen proactivamente estarán mejor posicionados cuando los Organismos Notificados y las agencias reguladoras comiencen a hacer referencia a ella en revisiones, formación y marcos de auditoría, lo que típicamente ocurre entre 6 y 18 meses después de la finalización.
Un informe de validez científica (SVR) documenta la asociación establecida entre un analito y una condición clínica específica, estado fisiológico o finalidad prevista. Constituye la base del paquete de evidencia clínica. Bajo el Anexo XIII del IVDR, un SVR ya es un componente obligatorio de la documentación técnica para IVD. N91 refuerza este requisito a nivel global y proporciona definiciones y expectativas actualizadas sobre cómo debe determinarse y documentarse la validez científica.